- Accueil
- Forums
- Forums généraux
- Recherche et liens utiles - Sclérose en plaques
- Liens utiles et recherches globales
Liens utiles et recherches globales
- 25 894 vues
- 2 014 soutiens
- 1 528 commentaires
Tous les commentaires
Aller au dernier commentaire

SepSepien
Bon conseiller
![]()
SepSepien
Dernière activité le 12/05/2026 à 12:35
Inscrit en 2018
3 311 commentaires postés | 1971 dans le groupe Recherche et liens utiles - Sclérose en plaques
492 de ses réponses ont été utiles pour les membres
Récompenses
-
Bon conseiller
-
Contributeur
-
Messager
-
Engagé
-
Explorateur
-
Evaluateur
@maritima @Chris31 , @ tous,
Question à mon neurologue :
1er mail avec résultats du labo.
La valeur pour les IgG anti EBNA est élevée. (doct joint)
J'ai eu besoin d'une référence pour tenter de comprendre les valeurs des tests. Le document suivant m'interpelle : https://www.doctissimo.fr/html/sante/analyses/sa_688_serologie_virale01.htm
Infection ancienne, j'espère, mais ne faut-il pas tester les IgG anti EA au vu du résultat ?
2è mail hier :
Bonsoir Docteur,
Un document attire mon attention : https://www.sciencedirect.com/science/article/pii/S1471491419302941
Traduction d'un passage :
<< Au cours des 20 dernières années, des études convergentes menées par plusieurs chercheurs ont mis en évidence un lien entre l'infection à EBV et le développement (c'est-à-dire l'étiologie) de la SEP [17, 18, 19, 20, 21]. La SEP ne se développe pas en l'absence d'exposition à l'EBV, et l'EBV est un facteur "nécessaire", mais insuffisant en soi, qui contribue à la pathophysiologie précoce de la maladie. Un soutien indépendant provient d'un taux d'activation de l'EBV plus élevé observé dans la SEP [22,23], d'un rôle de l'EBV dans le déclenchement de nouvelles rechutes correspondant à une capacité réduite des cellules T CD8+ spécifiques de l'EBV (par exemple, épuisement des cellules T, voir le glossaire) à limiter la réactivation de l'EBV chez les patients atteints de SEP [24,25], et d'une forte corrélation entre la présence d'anticorps anti-EBV dans le sang et l'apparition de la maladie [26, 27, 28, 29].
Les preuves de l'implication du SNC proviennent de rapports de sérologie anti-EBNA1 IgG élevée associée à l'apparition de nouvelles lésions cérébrales renforcées par le gadolinium (Gd) [30] et la présence, chez les patients, de cellules T spécifiques à EBNA1 reconnaissant la myéline [31].
En plus des cellules B infectées par l'EBV en périphérie qui contribuent à la récidive de la maladie, l'EBV peut jouer un rôle crucial dans la propagation de l'inflammation et des lésions compartimentées du SNC, contribuant potentiellement aux aspects progressifs (non récidivants) de la SEP. Les cellules B peuvent non seulement entrer dans le SNC, mais aussi en sortir pour pénétrer dans les ganglions lymphatiques cervicaux profonds [32,33].
Ces cellules B comprennent celles qui sont infectées par l'EBV, qui pourraient alors activer des réponses aberrantes des cellules T en périphérie. On peut supposer que l'EBV provenant des pools du SNC pourrait contribuer non seulement à l'inflammation compartimentée du SNC mais aussi à d'autres rechutes de la maladie.
À l'appui de cette affirmation, on trouve des preuves de la présence d'anticorps dans le liquide céphalorachidien (LCR) de patients atteints de SEP qui reconnaissent les antigènes de l'EBV [34], et des preuves que les lymphocytes B et les plasmocytes infectés par l'EBV s'accumulent dans le cerveau des personnes atteintes de SEP dans des collections de cellules immunitaires méningées (encadré 3). Bien que la présence de ces cellules B infectées par l'EBV dans le cerveau des personnes atteintes de SEP n'ait pas été observée dans toutes les études [35], la possibilité que ces cellules participent à des réactions de type centre germinal (GC) dans les méninges pourrait favoriser l'activation continue des cellules immunitaires et le maintien d'un pool de cellules pathogènes infectées par l'EBV dans le SNC. >>
Comment réagir à un taux d'anti-EBNA1 IgG élevé ?
(etc)
Je ne sais pas si cette valeur (689), bien plus élevée que le haut de la fourchette (320) serait en rapport avec une activité de ma SEP.
![]()

Voir la signature
Aut lux hic nata est, aut capta hic libera regnat.
![]()
maritima
Bon conseiller
![]()
maritima
Dernière activité le 12/05/2026 à 22:05
Inscrit en 2015
45 824 commentaires postés | 900 dans le groupe Recherche et liens utiles - Sclérose en plaques
16 332 de ses réponses ont été utiles pour les membres
Récompenses
-
Bon conseiller
-
Contributeur
-
Engagé
-
Explorateur
-
Evaluateur
-
Ami
La fin de ton message @SepSepien : c'est la question que je me poserais aussi ![]() ...... cette façon qu'on les labos de conclure de telle sorte que le questionnement soit plus présent après analyse qu'avant, c'est tout l'art de la fugue
...... cette façon qu'on les labos de conclure de telle sorte que le questionnement soit plus présent après analyse qu'avant, c'est tout l'art de la fugue ![]() ou de l'esquive à l'épée longue .
ou de l'esquive à l'épée longue .![]()
Infection ancienne ( Peut-on la dater ?Comment savoir si son début coïncide avec les premiers signes de la SEP?) ![]() !!!
!!!
Voir la signature
maritima. "l'amour pour épée, l'humour pour bouclier" Bernard Werber.

SepSepien
Bon conseiller
![]()
SepSepien
Dernière activité le 12/05/2026 à 12:35
Inscrit en 2018
3 311 commentaires postés | 1971 dans le groupe Recherche et liens utiles - Sclérose en plaques
492 de ses réponses ont été utiles pour les membres
Récompenses
-
Bon conseiller
-
Contributeur
-
Messager
-
Engagé
-
Explorateur
-
Evaluateur
@maritima à notre époque et depuis 40 ans, on sait que l'EBV déclenche la SEP (ou la PR chez d'autres patients).
Cela est très documenté et s'est précisé avec les années.
Des sites web font encore mine de le découvrir, c'est ahurissant.
95% de la population mondiale l'aura attrapé à une époque de sa vie, mais quasiment 100% des sépiens l'ont eu.
L'EBV déclencherait le processus auto-immun, de cette maladie qualifiée de "multifactorielle", car quand on manque de précisions, c'est le vocabulaire employé, tout comme on dit "idiopathique".
C'est dans les autres facteurs que la recherche s'éternise.
Il y a bien des chercheurs, qui précisent tel ou tel comportement biologique, mais les résultats tangibles n'arrivent pas, nous attendons vainement un traitement qui s'attaque aux causes et pas seulement à une phase intermédiaire de la réponse immunitaire.
L'analyse "standard" d'un labo se plie aux normes, le médecin lit et ne sort pas du protocole.
Il n'y a que quelques génies expérimentés, comme les professeurs sus-évoqués, pour communiquer autre chose que des lieux communs.
Le conformisme règne en maître, et tout ingénu curieux qui pose des questions qui dérangent, quand il n'est pas ignoré, se fait remettre à sa place.
Etant ingénu, curieux et malade, cela ne me dérange pas d'interroger médecins, les miens ou d'autres. Mais en refusant qu'on m'impose des recettes de supermarché ou des plats préparés.
C'est de la (haute-)cuisine que je demande aux chercheurs (ceux qui savent ...).
Le serment d'Hippocrate voudrait que chaque médecin ait de l'empathie, l'envie d'aider ses patients, ... on en trouve et mon médecin traitant en est un exemple parfait. Mon neurologue répond de bonnes grâces. Mais ils ne sont pas chercheurs et ont beaucoup de travail. Tout comme mon labo qui a été débordé avec le COVID-19.
Bises et amitiés !![]() !!!!!
!!!!!
Voir la signature
Aut lux hic nata est, aut capta hic libera regnat.

SepSepien
Bon conseiller
![]()
SepSepien
Dernière activité le 12/05/2026 à 12:35
Inscrit en 2018
3 311 commentaires postés | 1971 dans le groupe Recherche et liens utiles - Sclérose en plaques
492 de ses réponses ont été utiles pour les membres
Récompenses
-
Bon conseiller
-
Contributeur
-
Messager
-
Engagé
-
Explorateur
-
Evaluateur
@maritima j'ai bon souvenir d'une MNI attrapée (verre d'eau d'un restau sentant la bave) vers mai 1993. Où sont passées mes traces ? ... 2 papiers me manquent, dommage.
Il y a un topo précis sur https://medicalforum.ch/fr/journalfile/view/article/ezm_smf/fr/fms.2014.01831/145e569fd4976c2aad69fcdcc90e908f350c6206/fms_2014_01831.pdf/rsrc/jf et un rapport établi avec les MAI p.7.
On peut lire aussi http://www.chu-charleroi.be/RMC/Render.aspx?doc=fSeERrCAuZ9Bvlh7ukB97w==&crc=4hVkv5P7ZA4ZcEYqvhoAUQ2
... même si la médecine n'est pas une science exacte, il y a consensus : http://www.ligue-sclerose.fr/Actualites/Une-serologie-EBV-negative-pourrait-exclure-une-SEP
Au fait, je sais que tu sais, c'est juste pour partager ...
![]() !!!
!!!
Voir la signature
Aut lux hic nata est, aut capta hic libera regnat.
![]()
maritima
Bon conseiller
![]()
maritima
Dernière activité le 12/05/2026 à 22:05
Inscrit en 2015
45 824 commentaires postés | 900 dans le groupe Recherche et liens utiles - Sclérose en plaques
16 332 de ses réponses ont été utiles pour les membres
Récompenses
-
Bon conseiller
-
Contributeur
-
Engagé
-
Explorateur
-
Evaluateur
-
Ami
ET la MNI attrapée c'était le verre d'eau ![]() et .... malgré qq doute tu as bu quand même ?!!! et sauf pbs bucco-dentaires je pensais que la bave ( salive?) ne sentait rien .....
et .... malgré qq doute tu as bu quand même ?!!! et sauf pbs bucco-dentaires je pensais que la bave ( salive?) ne sentait rien ..... ![]() !!!
!!!
Voir la signature
maritima. "l'amour pour épée, l'humour pour bouclier" Bernard Werber.

SepSepien
Bon conseiller
![]()
SepSepien
Dernière activité le 12/05/2026 à 12:35
Inscrit en 2018
3 311 commentaires postés | 1971 dans le groupe Recherche et liens utiles - Sclérose en plaques
492 de ses réponses ont été utiles pour les membres
Récompenses
-
Bon conseiller
-
Contributeur
-
Messager
-
Engagé
-
Explorateur
-
Evaluateur
@maritima , la MNI ne s'attrape pas que dans le baiser, la salive est un vecteur très connu pour la contagion ... et les verres (mal lavés) y contribuent. A 28 ans, je n'imaginais pas tout cela. Un verre mal lavé sent "le chien" .
En tous cas, ( @Chris31 et tous, aussi) bonne nouvelle, du 25/6, GeNeuro a repris ses tests : http://www.geneuro.com/data/news/2020.06.25-GeNeuro-CP-MSResumption-FR-VF.pdf
GeNeuro annonce le recrutement du premier patient dans l'essai clinique de phase 2 évaluant le temelimab dans la sclérose en plaques en collaboration avec le Academic Specialist Center du Karolinska Institutet
Genève, Suisse, le 25 juin 2020 – 07h30 CEST - GeNeuro (Euronext Paris : CH0308403085 – GNRO), société biopharmaceutique qui développe de nouveaux traitements ciblant des facteurs clés dans la progression des maladies neurodégénératives et des maladies auto-immunes, notamment la sclérose en plaques (SEP) et la sclérose latérale amyotrophique (SLA), annonce aujourd'hui le recrutement du premier patient dans son essai clinique de phase 2 évaluant le temelimab dans la SEP à l’Academic Specialist Center (ASC) du Karolinska Institutet, à Stockholm, en Suède.
Argumentaire : http://www.geneuro.com/fr/technologies-fr/rationnel
et quand j'arrive à envoyer un lien à mes contacts, maintenant c'est ce lien : https://www.sciencedirect.com/science/article/pii/S0165247819303359?via%3Dihub encore faut-il qu'ils le lisent ...
Peptides de liaison HLA DR2b de l'enveloppe du rétrovirus endogène humain, du virus Epstein-Barr et des protéines cérébrales dans le contexte du mimétisme moléculaire de la sclérose en plaques
... noter aussi https://www.sciencedirect.com/science/article/pii/S1471491419302941 dont voici un extrait :
Sclérose en plaques et VEB : évolution de la théorie
La sclérose en plaques est une maladie chronique à médiation immunitaire dont l'étiologie est complexe, impliquant un système immunitaire dérégulé avec des épisodes d'inflammation à médiation périphérique, ainsi qu'une inflammation continue du système nerveux central (SNC), qui conduit à la perte de tissu neural et à l'aggravation du handicap [1,2]. Des vagues intermittentes de régulation et/ou d'activation aberrantes de sous-ensembles de cellules immunitaires entraînent leur trafic et leur infiltration périvasculaire à travers la barrière hémato-encéphalique (BHE) dans le SNC où les cellules immunitaires sont réactivées et ont un impact sur le tissu sous-jacent, ce qui entraîne des rechutes de la maladie. Les fondements biologiques de la SEP progressive non récurrente ne sont pas bien compris, mais on pense qu'elle est due, au moins en partie, à une inflammation du SNC impliquant la persistance des cellules immunitaires et leur activation autour des lésions périvasculaires et dans les méninges. En ce qui concerne l'étiologie de la SEP, on pense que la susceptibilité génétique et les expositions environnementales sont toutes deux impliquées [3, 4, 5]. L'incidence à vie de la SEP dans la population générale varie entre 2,0 et 9,6 pour 100 000 patients-années. Le taux de concordance de la SEP chez les jumeaux génétiquement identiques, qui va de ∼30% dans les populations du nord à 15%, voire 6% dans des pays comme l'Italie et la France, souligne non seulement la contribution du risque génétique mais aussi l'importance de l'action de l'environnement sur un hôte génétiquement prédisposé. Il a été démontré que les interactions entre les cellules T et, plus récemment, les cellules B, jouent un rôle crucial dans l'apparition de nouvelles rechutes [6, 7, 8, 9, 10]. Le contrôle très efficace de la maladie observé grâce à l'anticorps anti-cellules B, l'ocrelizumab, renforce l'intérêt pour le développement de traitements supplémentaires à médiation cellulaire. En s'appuyant sur le succès de ces études, on pourrait concevoir et mettre en œuvre une approche ciblant le rôle implicite d'un virus à cellules B dans la sclérose en plaques.
Des expositions environnementales spécifiques sont pertinentes à la fois pour déclencher la SEP et pour moduler l'évolution de la maladie. L'infection virale est un facteur environnemental crucial. De tous les virus considérés dans la pathogenèse de la SEP, l'EBV, un virus à forte concentration de cellules B, est le plus étudié (tableau 1). Le contrôle défectueux de l'EBV est associé à la mononucléose infectieuse (MI) en plus du lymphome de Hodgkin, du lymphome de Burkitt, du cancer gastrique, du carcinome nasopharyngé et des affections associées au VIH, telles que la leucémie à cellules ciliées et d'autres lymphomes [11,12]. Il est également prouvé que l'infection par l'EBV et les associations avec des facteurs de transcription, impliquant l'antigène nucléaire 2 de l'EBV (EBNA2), opérant dans différents loci de maladie, sont liées à un risque plus élevé de maladies auto-immunes autres que la SEP, y compris le lupus érythémateux systémique, l'arthrite rhumatoïde et le syndrome de Sjögren [13, 14, 15, 16].
Traduit avec www.DeepL.com/Translator (version gratuite)
Voilà, c'est la page la plus importante pour moi de la file.
![]() !!!
!!!
Voir la signature
Aut lux hic nata est, aut capta hic libera regnat.

SepSepien
Bon conseiller
![]()
SepSepien
Dernière activité le 12/05/2026 à 12:35
Inscrit en 2018
3 311 commentaires postés | 1971 dans le groupe Recherche et liens utiles - Sclérose en plaques
492 de ses réponses ont été utiles pour les membres
Récompenses
-
Bon conseiller
-
Contributeur
-
Messager
-
Engagé
-
Explorateur
-
Evaluateur
Bonjour @maritima @Chris31 @Guerrison , @tous,
Voici un article de 2015 : il étudie les liens entre SEP et le système du complément (protéine C3, ...) : https://scleroseenplaques.ca/nouvelles-sur-la-recherche/article/des-chercheurs-etablissent-un-lien-entre-le-systeme-du-complement-partie-integrante-du-reseau-immunitaire-et-la-progression-de-la-sclerose-en-plaques
On peut pousser plus loin.
En l'état, je souhaite réduire mes interventions, la priorité étant l'exercice physique.
Rien à attendre des communications avec les chercheurs français.
C'est donc ce qui est en rapport avec l'article https://www.sciencedirect.com/science/article/pii/S0165247819303359?via%3Dihub et avec le temelimab qui retient le plus mon attention.
N'étant pas médecin, je ne vais pas m'y mettre plus encore ...
Bises et amitiés.![]()
Voir la signature
Aut lux hic nata est, aut capta hic libera regnat.

SepSepien
Bon conseiller
![]()
SepSepien
Dernière activité le 12/05/2026 à 12:35
Inscrit en 2018
3 311 commentaires postés | 1971 dans le groupe Recherche et liens utiles - Sclérose en plaques
492 de ses réponses ont été utiles pour les membres
Récompenses
-
Bon conseiller
-
Contributeur
-
Messager
-
Engagé
-
Explorateur
-
Evaluateur
Bonjour @maritima @Chris31 @Guerrison , @tous,
Cet article du 5 mai (révisé le 22/5/2020) de 65 pages me captive ... mais je le savoure doucement : https://www.mdpi.com/2076-3425/10/6/333/htm
Traduit avec www.DeepL.com/Translator (version gratuite)
Avancées récentes dans le domaine des immunothérapies antigènes spécifiques pour le traitement de la sclérose en plaques
par Olga Kammona et Costas Kiparissides - Grèce (rédigé en anglais).
EXTRAITS :
Résumé
La sclérose en plaques (SEP) est une maladie auto-immune du système nerveux central et est considérée comme la principale cause non traumatique de handicap neurologique chez les jeunes adultes. Les traitements actuels de la SEP comprennent des médicaments immunosuppresseurs à long terme et des thérapies de modification de la maladie (DMT) conçues pour modifier sa progression avec un risque accru d'effets secondaires graves. Le Saint Graal pour le traitement de la SEP est de supprimer spécifiquement la maladie tout en permettant au système immunitaire d'être fonctionnellement actif contre les maladies infectieuses et la malignité. Cela pourrait être réalisé par le développement d'immunothérapies conçues pour supprimer spécifiquement les réponses immunitaires aux auto-antigènes (par exemple, les antigènes de la myéline). La présente étude tente de mettre en évidence les différentes immunothérapies spécifiques aux antigènes développées jusqu'à présent pour le traitement de la sclérose en plaques (par exemple, vaccination avec des peptides/protéines dérivés de la myéline, ADN plasmidique codant pour les épitopes de la myéline, cellules dendritiques tolérantes pulsées avec des épitopes encéphalitogènes de protéines de la myéline, cellules T autologues atténuées spécifiques des antigènes de la myéline, peptides des récepteurs des cellules T, porteurs chargés/conjugués avec des peptides immunodominants de la myéline, etc. ), en se concentrant sur les résultats de leur récente évaluation préclinique et clinique, et pour faire la lumière sur les mécanismes impliqués dans l'immunopathogénèse et le traitement de la sclérose en plaques."
...
2. Immunopathogénèse de la SEP
Les études précliniques et les essais cliniques réussis pour la SEP qui ciblent les cellules et les molécules du système immunitaire soutiennent l'idée que ce dernier a un rôle dominant dans la pathogénie de la SEP. Ces études ont montré que les cellules du système immunitaire adaptatif, comme les cellules B et les divers lymphocytes T effecteurs, combinées aux cellules du système immunitaire inné, comme les cellules tueuses naturelles et les microglies, contribuent de manière unique à la maladie [2]. Toutefois, il convient de mentionner que si le système immunitaire adaptatif périphérique (lymphocytes T) est le principal moteur de la SEP-RR, le système immunitaire inné (microglies et astrocytes), associé aux lymphocytes B, est considéré comme le moteur de la SEP progressive [2]. Le SNC des patients atteints de SEP présente également une infiltration de lymphocytes T, de lymphocytes B, de plasmocytes, de cellules dendritiques (CD) et de macrophages activés, indiquant la contribution des réponses immunitaires cellulaires et humorales (c'est-à-dire médiées par des anticorps) ainsi que de divers mécanismes effecteurs immunopathologiques à l'endommagement des tissus du SNC [22,23].
Il a été suggéré que deux types d'inflammation indépendants, se développant en parallèle, peuvent se produire chez les patients atteints de sclérose en plaques. Le premier est lié à l'invasion focale des cellules T et B par les fuites de BHE, donnant lieu à des plaques démyélinisées actives classiques dans la substance blanche. La seconde concerne une lente accumulation de lymphocytes T et B sans lésion profonde de la BHE dans les espaces périvasculaires de Virchow Robin et les méninges, où ils forment des agrégats cellulaires ressemblant, dans les cas les plus graves, à des follicules lymphatiques tertiaires. Ces derniers peuvent être liés au développement de lésions démyélinisées dans le cortex cérébral et cérébelleux, à la lente expansion des lésions existantes dans la substance blanche et à une neurodégénérescence diffuse dans la substance blanche et/ou grise d'apparence normale [18]. La présence de structures lymphoïdes de type follicule (centres germinaux ectopiques de type follicule) dans les méninges cérébrales enflammées de certains patients atteints de SEP-SP pourrait indiquer que la maturation des lymphocytes B est soutenue localement dans le SNC et contribue à l'induction d'une réponse immunitaire humorale compartimentée [2,22].
Le rôle des différentes cellules immunitaires et les mécanismes effecteurs immunopathologiques contribuant au développement de la SEP sont abordés ci-dessous.
La capacité du système immunitaire humain à répondre à un très grand nombre d'antigènes rencontrés s'accompagne du risque que certains lymphocytes T soient capables de reconnaître des auto-antigènes, tels que les antigènes du SNC (par exemple, la myéline). La plupart des lymphocytes T autoréactifs sont généralement supprimés dans le thymus par un processus connu sous le nom de sélection négative (tolérance centrale). Cependant, un certain nombre de ces lymphocytes T s'échappent du thymus vers des sites périphériques où ils sont normalement maintenus sous contrôle par des mécanismes de tolérance périphérique. Si ces mécanismes échouent, en raison d'une action réduite des cellules T régulatrices et/ou d'une résistance accrue des lymphocytes T et B effecteurs à la suppression, les cellules T autoréactives reconnaissant les antigènes du SNC sont activées dans le système lymphoïde périphérique pour devenir des cellules effectrices, par mimétisme moléculaire (c'est-à-dire activation par un peptide viral ayant une similarité de séquence suffisante [24] ou partageant un épitope immunologique [25] avec l'antigène du SNC), la reconnaissance des protéines du SNC libérées dans la périphérie, la présentation de nouveaux auto-antigènes et l'activation par des spectateurs (c'est-à-dire l'activation indépendante du récepteur des cellules T (TCR) et dépendante des cytokines, probablement due à une infection virale [26]). Ensuite, les cellules T activées (les cellules T CD8+ et CD4+ se différencient en cellules T auxiliaires 1 (Th1) et Th17) ainsi que les cellules B et les monocytes (cellules du système immunitaire inné) s'infiltrent dans le SNC en traversant la barrière hémato-encéphalique (BHE), ce qui entraîne une inflammation. Là, ils sont réactivés par les cellules résidentes présentant des antigènes, les APC (par exemple, les cellules microgliales) et les APC infiltrantes (par exemple, les cellules dendritiques, les macrophages) présentant des autoantigènes du SNC sur les molécules du complexe majeur d'histocompatibilité, CMH (également connu sous le nom d'antigène leucocytaire humain, HLA, chez l'homme [11]). Plus précisément, les cellules T CD4+ interagissent avec les cellules exprimant le CMH II, comme les cellules dendritiques, les macrophages et les cellules B, tandis que les cellules T CD8+ interagissent directement avec les cellules exprimant l'antigène du CMH I, comme les neurones et les oligodendrocytes. Il convient de noter que le CMH de classe II n'est adéquatement exprimé que sur les APC professionnelles, tandis que le CMH de classe I est exprimé par tous les types de cellules du milieu inflammatoire du SNC. Par conséquent, les cellules T CD4+ se trouvent principalement dans les brassards périvasculaires et les méninges, tandis que les cellules T CD8+ infiltrent en outre le parenchyme des lésions irritées. Au contact de leur antigène apparenté, les cellules T CD4+ sont censées sécréter des cytokines et des médiateurs immunitaires, ce qui entraîne l'attraction de cellules immunitaires résidentes comme les microglies, les macrophages et les astrocytes, la sécrétion de cytokines pro-inflammatoires, une fonction APC renforcée et une production accrue d'espèces réactives d'oxygène et d'azote (ROS/RNS). D'autre part, outre la sécrétion de cytokines pro-inflammatoires, l'amélioration de la fonction APC et l'augmentation de la production d'espèces réactives d'oxygène et d'azote (ROS/RNS).
D'autre part, outre la sécrétion de médiateurs inflammatoires, les cellules T CD8+ attaquent directement les oligodendrocytes et les neurones, provoquant ainsi la mort des oligodendrocytes (par exemple, via la sécrétion de granzymes et de perforine entraînant la formation de pores et la stimulation de la mort cellulaire programmée [2]) et des lésions neuronales (par exemple, la libération de granules cytolytiques entraînant la dissection axonale [2]) (Figure 2). Les phénomènes ci-dessus entraînent une inflammation, une perte de myéline et des lésions axonales. Cette cascade inflammatoire conduit au recrutement de monocytes et de macrophages dans la lésion, ce qui entraîne la libération d'un plus grand nombre d'antigènes du SNC et leur présentation à des cellules T potentiellement autoréactives. Il convient de mentionner que la propagation des épitopes pourrait entraîner une réponse auto-immune plus large impliquant des auto-antigènes supplémentaires.
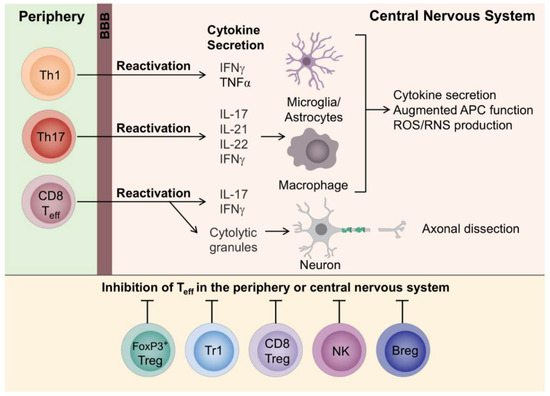
(Figure 2 : Les cellules T effectrices dans la sclérose en plaques )
Les cellules T CD4+ sont considérées comme ayant un rôle primordial dans l'immunopathogénèse de la SEP en raison de la sécrétion de l'interféron gamma (IFNγ) et de l'IL-17 [2,20,34]. Cependant, il a été récemment révélé que les cellules T CD8+ sont également responsables de l'initiation de la pathogénèse de la SEP humaine où, contrairement à l'encéphalomyélite auto-immune expérimentale (EAE), les cellules T CD8+ sont le lymphocyte T prédominant infiltré dans les lésions aiguës et chroniques de la SEP [1,2]. Par rapport aux cellules T CD4+, les cellules T CD8+ se trouvent plus fréquemment dans la substance blanche et dans les lésions de démyélinisation corticale de la substance grise, et leur densité peut être étroitement corrélée aux lésions axonales [1,3]. On a constaté que la propagation des épitopes, assistée par la présentation croisée des antigènes par les CD dérivées des monocytes, active les cellules T CD8+ spécifiques de la myéline, également dans un modèle d'EAE [3]. Il a été suggéré que les cellules T CD8+ restent dans le SNC (par exemple, le cerveau et la moelle épinière) en tant que cellules résidant dans les tissus, et lors de la rencontre de leur antigène apparenté, propagent la neuroinflammation de manière focalisée [18].
Bien que la SEP soit considérée comme une maladie à médiation lymphocytaire T (35), les résultats importants du traitement anti-CD20 (par exemple, rituximab, ocrelizumab) de la SEP indiquent un rôle significatif des cellules B dans sa pathogénie. Les cellules B peuvent avoir un rôle pro- ou anti-inflammatoire, selon leur sous-type et leur contexte. Leurs fonctions pro-inflammatoires comprennent la présentation critique de l'antigène dans le contexte des molécules du CMH de classe II aux cellules Th17 et Th1, la sécrétion de cytokines pro-inflammatoires (par exemple, le facteur de nécrose tumorale alpha, TNF-α, l'interleukine-6 (IL-6) et le facteur de stimulation des colonies de granulocytes-macrophages, GM-CSF) qui favorisent l'inflammation du SNC et propagent la démyélinisation et la neurodégénérescence, et la production d'anticorps [36]. Les lymphocytes B peuvent quitter le SNC pour se rendre aux ganglions lymphatiques cervicaux où ils peuvent subir une maturation d'affinité, puis revenir dans le SNC et provoquer d'autres lésions [3].
Les lymphocytes B sont considérés comme une population unique d'APC car, contrairement aux autres APC qui reconnaissent divers antigènes exogènes et endogènes, les lymphocytes B sont hautement sélectifs (c'est-à-dire qu'ils ne reconnaissent spécifiquement que les antigènes qui sont liés à leur récepteur unique de surface des lymphocytes B). Des études réalisées avec le modèle EAE ont indiqué que certains autoantigènes, comme la glycoprotéine oligodendrocyte de myéline (MOG) hautement immunogène, nécessitent leur présentation par les cellules B pour activer les cellules T CD4+. En conséquence, on peut supposer que le ou les antigènes qui déclenchent la SEP humaine sont également dépendants des cellules B [36]. De plus, les gènes actifs dans les cellules B représentent un composant majeur de plus de 200 variantes connues pour augmenter le risque de développer la SEP. Fait remarquable, le gène qui code la chaîne DR β du CMH de classe II, dont on sait qu'elle est essentielle à la fonction APC, est considéré, à l'échelle du génome, comme le plus fort signal de prédisposition à la SEP. L'effet net de cette charge génétique est probablement une biologie biaisée des cellules B vers un phénotype pro-inflammatoire, qui favorise la présentation d'auto-antigènes aux cellules T effectrices ou augmente les réponses auto-immunes par la production de cytokines et autres médiateurs immunitaires [36].
Les cellules T régulatrices (CD4 FoxP3+ Tregs, CD4+ Tr1, CD8 Tregs), les cellules B régulatrices (Breg) et les cellules tueuses naturelles (cellules NK) peuvent réguler les cellules T effectrices dans le tissu lymphoïde périphérique ou dans le SNC. Les FoxP3+ Tregs CD4 (<4% des cellules T CD4 circulantes) expriment le facteur de transcription Forkhead box protein 3 (FoxP3) ainsi que de nombreuses molécules inhibitrices à leur surface. Elles sont activées par des auto-antigènes et suppriment l'activation d'autres types de cellules par un mécanisme qui nécessite un contact cellulaire [37]. Les cellules régulatrices CD4+ Tr1 entravent la prolifération cellulaire principalement par la sécrétion d'IL-10 [38]. Les deux Tregs sont considérées comme importantes dans la SEP en raison de leurs caractéristiques uniques. Des sous-ensembles de Tregs CD8+ qui ont été indiqués pour supprimer les réponses immunitaires et la progression de la maladie par des mécanismes distincts ont été identifiés par une expression unique de molécules comme CD122, CD28, CD102 et HLA-G [2,39,40]. De plus, les cellules Th2 sécrétant des cytokines comme l'IL-4, l'IL-5 et l'IL-13 sont considérées comme capables de réguler à la baisse l'activité des cellules pro-inflammatoires [27]. Les cellules B peuvent également réguler diverses fonctions immunitaires effectrices médiées par les cellules B et T via la sécrétion de cytokines régulatrices IL-10 et IL-35, le facteur de croissance transformant bêta (TGF-β), ou le ligand de mort programmé 1 (PD-L1). Plus précisément, les IL-10 sécrétant des lymphocytes B inhibent les réponses pro-inflammatoires des lymphocytes T, en partie par l'intermédiaire de IFNγ et de l'IL17 [2,3,36]. Enfin, les cellules NK sont connues pour supprimer les réponses immunitaires en tuant les cellules T CD4+ activées, éventuellement pathogènes.
Des réseaux immunomodulateurs sont déclenchés parallèlement à l'activité délétère des cellules T effectrices, afin de limiter l'inflammation du SNC et d'amorcer la réparation des tissus, ce qui entraîne une remyélinisation partielle. La modulation de l'activation immunitaire peut être associée à une rémission clinique. Cependant, il convient de mentionner qu'en l'absence de traitement, la suppression de l'auto-immunité ne peut être totalement réalisée. Par conséquent, des attaques supplémentaires conduiront normalement à la forme progressive de la SEP [2]. L'action des cellules T et B autoréactives dans la SEP pourrait être due à la fonction défectueuse des cellules régulatrices. Les variants HLA de classe II associés à la maladie pourraient biaiser la sélection dans le thymus de sorte que les cellules T régulatrices qui sont libérées dans les sites périphériques ne peuvent pas supprimer de manière adéquate les cellules T effectrices autoréactives [3].
...
![]() !!!
!!!
Voir la signature
Aut lux hic nata est, aut capta hic libera regnat.
![]()
maritima
Bon conseiller
![]()
maritima
Dernière activité le 12/05/2026 à 22:05
Inscrit en 2015
45 824 commentaires postés | 900 dans le groupe Recherche et liens utiles - Sclérose en plaques
16 332 de ses réponses ont été utiles pour les membres
Récompenses
-
Bon conseiller
-
Contributeur
-
Engagé
-
Explorateur
-
Evaluateur
-
Ami
Savoure @SepSepien ![]() savoure !...... sauf que que ce n'est qu'à petites doses qu'on peut apprécier ! ça ne s'assimile pas à la première lecture !
savoure !...... sauf que que ce n'est qu'à petites doses qu'on peut apprécier ! ça ne s'assimile pas à la première lecture ! ![]() !!!
!!!
Voir la signature
maritima. "l'amour pour épée, l'humour pour bouclier" Bernard Werber.

SepSepien
Bon conseiller
![]()
SepSepien
Dernière activité le 12/05/2026 à 12:35
Inscrit en 2018
3 311 commentaires postés | 1971 dans le groupe Recherche et liens utiles - Sclérose en plaques
492 de ses réponses ont été utiles pour les membres
Récompenses
-
Bon conseiller
-
Contributeur
-
Messager
-
Engagé
-
Explorateur
-
Evaluateur
@maritima je ne peux comprendre en détails, tu le sais, il faut une formation.
Mais petit bout après petit bout, l'intuition se nourrit.
Ce qui serait bon, serait que des pros étudient cela, mais les destinées sont déjà tracées en France ... on n'imposera pas une lecture à ceux qui n'en veulent pas. A moins qu'ils aient déjà lu cette étude. J'en doute encore. Et qu'en f(er)ont-ils ?
![]() !!!
!!!
Voir la signature
Aut lux hic nata est, aut capta hic libera regnat.
Donnez votre avis
Articles à découvrir...

18/04/2026 | Nutrition
Entre promesses et réalité : les oméga-7 peuvent-ils améliorer la santé métabolique ?
S'abonner
Vous souhaitez être alerté des nouveaux commentaires
Votre abonnement a bien été pris en compte







SepSepien
Bon conseiller
SepSepien
Dernière activité le 12/05/2026 à 12:35
Inscrit en 2018
3 311 commentaires postés | 1971 dans le groupe Recherche et liens utiles - Sclérose en plaques
492 de ses réponses ont été utiles pour les membres
Récompenses
Bon conseiller
Contributeur
Messager
Engagé
Explorateur
Evaluateur
@sasufi
information complètement mise en doute par la communauté médicale et pas seulement française :
https://www.allodocteurs.fr/vaccins-et-sclerose-en-plaques-le-vrai-du-faux-34025.html
Plusieurs vaccins sont souvent soupçonnés de jouer un rôle dans l'apparition d'une sclérose en plaques. Pourtant, aucun lien n'existe entre la vaccination et cette maladie neurologique. On vous explique.