- Accueil
- Forums
- Forums généraux
- Bon à savoir (pour tous)
- Avancé médicale et nouveaux traitements
Avancé médicale et nouveaux traitements
- 589 vues
- 31 soutiens
- 77 commentaires
Tous les commentaires
Aller au dernier commentaire

dinouille
Membre AmbassadeurBon conseiller
![]()
dinouille
Membre Ambassadeur
Dernière activité le 27/04/2026 à 09:14
Inscrit en 2015
133 819 commentaires postés | 107578 dans le groupe Bon à savoir (pour tous)
31 091 de ses réponses ont été utiles pour les membres
Récompenses
-
Bon conseiller
-
Contributeur
-
Messager
-
Engagé
-
Explorateur
-
Evaluateur
SANTÉCancers du sang : un traitement révolutionnaire autorisé en France
Une technique qui consiste à modifier génétiquement les globules blancs des malades pour qu'ils s'attaquent aux tumeurs vient d'être autorisée dans deux hôpitaux parisiens.
Le 15/08/2018 à 07:35
#Cancer du sang : 1ers succès d'un traitement par #immunothérapie "CAR-T"
22 patients atteints de #leucémies aiguës et de #lymphomes (B), ont bénéficié #thérapie #génique par cellules « #CAR-T » Une avancée relayée dans le @NEJM @APHP https://www.reseau-chu.org/article/cancer-du-sang-1ers-succes-dun-traitement-par-immunotherapie- #CAR-T » Une avancée relayée dans le @NEJM @APHP https://www.reseau-chu.org/article/cancer-du-sang-1ers-succes-dun-traitement-par-immunotherapie-car-t/ …
Un nouveau traitement révolutionnaire, capable de combattre les leucémies, les lymphomes et d'autres maladies du sang, vient d'être autorisé dans deux hôpitaux parisiens.
Les établissements Saint-Louis et Robert-Debré viennent d'être labellisés "centres experts pour le traitement par cellules CAR-T" et vont pouvoir proposer cette thérapie génique qui consiste à prélever le sang du patient, en extraire les globules blancs, les modifier génétiquement pour qu'ils s'attaquent aux tumeurs, les multiplier et les réinjecter dans son organisme.
Jusqu'à présent, le recours à cette technique n'était possible que dans le cadre d'essais cliniques.
La "découverte de l'année"
L'Association américaine de cancérologie a qualifié ce traitement de "découverte de l'année".
L'ANSM (agence nationale de santé et du médicament) devrait prochainement délivrer l'autorisation de mise sur le marché à deux dispositifs distincts développés par les laboratoires Novartis et Gilead, selon le magazine "Sciences et avenir".
"Grâce à cette thérapeutique, le taux de rémission à trois ans des patients, enfants ou jeunes adultes (jusqu'à 25 ans) avec une leucémie aiguë réfractaire au traitement est de 83% contre 15% avec les traitements classiques. Pour les patients souffrant d'un lymphome diffus à grandes cellules B réfractaire, le taux de rémission complète à 15 mois est de 40 % contre 5 à 10 % avec une chimiothérapie conventionnelle", détaille l'AP-HP ('Assistance publique-Hôpitaux de Paris) dans un communiqué.
Un vrai espoir pour les malades : plus de 33 000 nouveaux cas sont diagnostiqués chaque année en France, les leucémies, lymphomes, myélomes étant les cancers du sang les plus fréquents.
La leucémie aigüe myéloïde, le cancer du sang le plus fréquent et le plus agressif chez l'adulte, est incurable chez la plupart des patients.
LES DIFFÉRENTS CANCERS DU SANG
La moelle osseuse (à ne pas confondre avec la moelle épinière) se trouve dans les os plats : crâne, os iliaque, côtes, sternum et colonne vertébrale. C’est là que se forment les trois types de cellules du sang :
-les globules rouges (ou érythrocytes) ;
-les globules blancs (ou leucocytes) ;
-les plaquettes.
Selon le site internet de l'institut Curie, les cancers "hématologiques", développés à partir de ces cellules du sang, sont dus à des altérations survenues à différents stades de leur maturation et qui favorisent leur prolifération.
On distingue trois grandes familles de cancers du sang :
-les leucémies, caractérisées le plus souvent par la présence de cellules anormales circulant dans le sang ;
-les myélomes, qui se manifestent notamment par des lésions osseuses,
-les lymphomes, qui touchent principalement les ganglions.
Voir la signature
dinouille

dinouille
Membre AmbassadeurBon conseiller
![]()
dinouille
Membre Ambassadeur
Dernière activité le 27/04/2026 à 09:14
Inscrit en 2015
133 819 commentaires postés | 107578 dans le groupe Bon à savoir (pour tous)
31 091 de ses réponses ont été utiles pour les membres
Récompenses
-
Bon conseiller
-
Contributeur
-
Messager
-
Engagé
-
Explorateur
-
Evaluateur
Paiement 100% sécurisé
Douleur : une nouvelle cible thérapeutique dans la spasticité et la douleur chronique liées à une lésion de la moelle épinière
Les lésions de la moelle épinière génèrent dans 70 % des cas une spasticité associée à une douleur chronique.
Ces symptômes sont particulièrement préjudiciables pour les patients, au point d’être plus gênants que la paralysie elle-même.
Les chercheurs ont mis en évidence le rôle d’une protéine dans ces symptômes, et ils souhaitent aujourd’hui savoir si elle constitue une cible thérapeutique potentielle.
Ce projet est mené par Irène Sanchez dans l’équipe « Plasticité et physio-pathologie des réseaux moteurs rythmiques » (P3M) dirigée par Frédéric Brocard à l’Institut de Neurosciences de la Timone à Marseille.
Douleur, spasticité et lésion de la moelle épinière
Après lésion de la moelle épinière, près de 70 % des personnes souffrent de douleurs chroniques et de spasticité. La spasticité est caractérisée par l’augmentation de certains réflexes sensoriels ou moteurs, une raideur musculaire, une contraction des muscles accrue et des spasmes. Douleur et spasticité se développent graduellement au cours des mois et des années qui suivent la lésion, au point de devenir plus négatifs pour les malades que la paralysie elle-même. Les traitements disponibles étant le plus souvent inefficaces, les recherches dans ce domaine restent donc indispensables afin de soulager les personnes atteintes.
Quels sont les mécanismes neuronaux impliqués ?
Les échanges de messages entre le cerveau et les muscles via la moelle épinière sont transmis au travers d’un réseau de neurones. Il en existe deux types : les neurones « excitateurs » (relayant par exemple la contraction) et les réseaux « inhibiteurs » (correspondant au signal du relâchement). En conditions normales, ces deux systèmes fonctionnent en équilibre. En revanche, les scientifiques pensent qu’en cas de lésion de la moelle épinière, l’inhibition des circuits neuronaux est réduite et, à l’inverse, l’action des neurones excitateurs est plus importante. Ce phénomène serait au cœur de la spasticité musculaire et des douleurs associées.
La protéine KCC2 en cause
Irène Sanchez s’intéresse à des protéines neuronales appelées KCC2 qui sont impliquées dans le phénomène d’inhibition. La production de ces protéines est diminuée suite à une lésion de la moelle épinière, et leur absence entraîne une diminution de l’inhibition neuronale. Les chercheurs veulent donc stimuler la production des protéines KCC2 afin de restaurer l’inhibition neuronale perdue chez les patients.
Test de deux composés pharmacologiques
L’équipe a identifié deux composés pharmacologiques qui seraient en mesure d’augmenter la production de KCC2 et donc de compenser la perte de l’inhibition neuronale : ces composés sont TCB2 et les molécules de la famille des phénothiazines (de puissants psychotropes). Plus précisément, ils agiraient en restaurant l’expression de KCC2 au sein des neurones. Les chercheurs souhaitent au travers de ce projet mieux caractériser leurs effets par des techniques de biologie cellulaire et moléculaire, en vue d’élucider leur mode d’action dans l’organisme.
Si les hypothèses des chercheurs se confirment, cela ferait de KCC2 une cible thérapeutique possible pour traiter la spasticité et la douleur associées à des lésions de la moelle épinière : un réel espoir à l’avenir pour les patients.
Date de publication : 01/07/2018
Vos dons
en actions
34 008 €
Financement reçu en 2017 par Irène Sanchez pour une fin de thèse.
La maladie
Douleur
La prise en charge de la douleur fait partie intégrante des soins. Les chercheurs tentent d’en comprendre les mécanismes pour trouver de nouvelles thérapies.
Recherches
Douleur : explorer les mécanismes de transition d’une douleur aiguë à chronique
Douleur : Explorer certains aspects de la douleur chronique
Douleur : nouvelles pistes pour le traitement de la spasticité et des douleurs chroniques après lésion de la moelle épinière
Voir la signature
dinouille

dinouille
Membre AmbassadeurBon conseiller
![]()
dinouille
Membre Ambassadeur
Dernière activité le 27/04/2026 à 09:14
Inscrit en 2015
133 819 commentaires postés | 107578 dans le groupe Bon à savoir (pour tous)
31 091 de ses réponses ont été utiles pour les membres
Récompenses
-
Bon conseiller
-
Contributeur
-
Messager
-
Engagé
-
Explorateur
-
Evaluateur
Asthme : explorer ses mécanismes par imagerie
L’asthme est une maladie inflammatoire chronique dont les traitements actuels ne sont pas optimaux.
Des chercheurs ont montré qu’une protéine mutée, l’Interleukine-33, pourrait être impliquée dans la maladie.
Ils souhaitent aujourd’hui observer son action avec une technique d’imagerie avancée, et ainsi dégager des mécanismes immunitaires qui pourraient constituer des cibles thérapeutiques pertinentes.
Ce projet est mené par Emma Lefrançais dans l’équipe « Biologie Vasculaire : Cellules endothéliales, Inflammation et Cancer » dirigée par Jean-Philippe Girard à l’Institut de Pharmacologie et de Biologie Structurale de Toulouse.
L’asthme est une maladie fréquente et parfois sévère
L’asthme est une maladie inflammatoire des bronches qui concerne 4 millions de Français. Ce nombre est d’autant plus préoccupant qu’il est en constante augmentation : il a triplé au cours de ces 20 dernières années. De plus, l’Assurance Maladie estime que près de 1 000 personnes en décèderaient chaque année dans l’hexagone. Mais cette pathologie est également très présente dans le monde : 235 millions de personnes en seraient atteintes selon l’Organisation Mondiale de la Santé. Les traitements disponibles n’ont pourtant que très lentement progressé et actuellement, ils visent surtout à diminuer les symptômes de la maladie, manquent de spécificité et ont souvent des effets secondaires. Il est donc urgent de mieux comprendre la physiopathologie de l’asthme afin de développer de nouvelles thérapies plus adaptées. C’est l’objectif poursuivi par Emma Lefrançais au cours de ce projet.
Une protéine impliquée la maladie
L’asthme résulte d’une hyperréactivité des bronches : en réponse à certains stimuli, leur paroi s’enflamme, induisant une contraction des cellules musculaires qui les composent et la sécrétion d’un mucus. La pathologie est dite « multifactorielle » car elle dépend à la fois de facteurs environnementaux comme la présence d’allergènes (pollen, poils d’animaux…), de facteurs d’exacerbations (pollution, grippe, cigarette…) mais également de prédispositions génétiques.
Emma Lefrançais s’intéresse à cette dernière composante. Plus particulièrement, elle étudie une protéine appelée interleukine-33 (ou IL-33). Des recherches ont montré que des mutations dans le gène nécessaire à sa production sont associées au développement de l’asthme, mais, pour le moment, son mécanisme d’action n’est pas entièrement compris. L’IL-33 est une protéine essentielle dans l’inflammation : aussi, la chercheuse pense que la cibler pourrait-être une voie de traitement prometteuse.
Observer le tissu pulmonaire
Cette étude vise donc à identifier les cellules inflammatoires activées par l’IL-33 au cours de l’inflammation pulmonaire allergique, mais également lors d’infections virales à l’origine des crises d’asthme les plus graves. A cette fin, l’équipe dispose d’une technique d’imagerie innovante : l’imagerie intravitale du poumon. Elle permet d’observer le tissu pulmonaire in vivo de manière très précise, et ainsi de suivre en temps réel les cellules immunitaires impliquées dans l’inflammation pulmonaire.
Avec ce projet, les chercheurs espèrent mieux comprendre les mécanismes immunitaires associés à l’asthme mais surtout identifier de nouvelles cibles thérapeutiques pour les maladies allergiques respiratoires.
Date de publication : 01/05/2018
Voir la signature
dinouille

dinouille
Membre AmbassadeurBon conseiller
![]()
dinouille
Membre Ambassadeur
Dernière activité le 27/04/2026 à 09:14
Inscrit en 2015
133 819 commentaires postés | 107578 dans le groupe Bon à savoir (pour tous)
31 091 de ses réponses ont été utiles pour les membres
Récompenses
-
Bon conseiller
-
Contributeur
-
Messager
-
Engagé
-
Explorateur
-
Evaluateur
Ostéoporose : Découvrir de nouvelles cibles thérapeutiques
L’ostéoporose est une maladie caractérisée par une fragilisation du tissu osseux, ce qui augmente le risque de fracture.
Cette baisse de densité de l’os est liée à un dysfonctionnement de certaines cellules, les ostéoclastes.
Les chercheurs souhaitent découvrir des moyens de bloquer les actions de ces cellules en vue d’améliorer la prise en charge de la maladie.
Cette recherche est menée par Anne Blangy et son équipe « GTPases Rho et biologie des ostéoclastes » au Centre de Recherche en Biologie cellulaire de Montpellier.
Quelques données générales sur l’ostéoporose
L’ostéoporose est une maladie du tissu osseux qui aboutit à une fragilisation des os et à une augmentation du risque de fracture. Cette pathologie constitue un véritable problème de santé publique : en France, l’Assurance maladie estime qu’entre 2,5 et 3,5 millions de femmes souffrent d’une ostéoporose après la ménopause. La fréquence de cette pathologie augmente avec le vieillissement, et peut également toucher les hommes après 65 ans. Selon l’Inserm, 377 000 fractures osseuses par an seraient liées à la maladie.
Les principaux retentissements de l’ostéoporose résident dans la perte d’autonomie du patient : seule la moitié des patients de plus de 60 ans retrouvent une mobilité normale de la hanche après une fracture du col du fémur. Autant de données qui montrent toute l’importance de cette maladie.
Un équilibre subtil qui régule la vie de l’os
Durant la vie, l’os est en renouvellement permanent. Schématiquement, certaines cellules, les ostéoclastes, détruisent tout d’abord l’os. Elles y créent des trous, les lacunes. Par la suite, un autre type de cellules, les ostéoblastes, migrent vers les lacunes et utilisent du calcium pour reformer du tissu osseux. L’ensemble de ce processus est à l’équilibre, et est régi par une multitude de facteurs (hormonaux, moléculaires…). L'ostéoporose est due à une augmentation anarchique de l’activité des ostéoclastes : ces derniers, trop activés, détruisent l’os sans réparation ultérieure. Le tissu osseux perd en densité et le risque de fracture est augmenté.
Vers un blocage de la dégradation osseuse
L’équipe menée par Anne Blangy s’intéressent au mécanisme de résorption osseuse mis en place par les ostéoclastes. Ces derniers possèdent des sortes de ventouses, les podosomes, qui leur permettent de s’accrocher à l’os pour agir. L’équipe a montré avec l’aide d’un précédent financement de la Fondation pour la Recherche Médicale, qu’il est possible de déstabiliser ces ventouses afin de diminuer l’activité des ostéoclastes. A l’aide d’une molécule spécifique, ils ont notamment réussi à bloquer le mécanisme à l’origine de la dégradation osseuse initiée par les ostéoclastes chez l’animal en empêchant l’adhésion des cellules sur l’os.
Aujourd’hui, ils veulent identifier des nouvelles molécules qui régulent ce mécanisme. L’équipe utilisera à cette fin des techniques d’imagerie automatique et à très haute résolution et des technologies avancées d’identification de gènes. Les chercheurs espèrent découvrir de nouvelles cibles thérapeutiques et ouvrir ainsi la voie à des traitements innovants de l’ostéoporose, tout aussi efficaces mais avec moins d’effets indésirables que les médicaments actuels
La maladie
Ostéoporose
L’ostéoporose est une pathologie fréquente qui se traduit par une baisse de la densité du tissu osseux, augmentant du même coup sa fragilité et donc le risque de fracture. Cette pathologie est aujourd’hui de mieux en mieux dépistée et sa prise en charge est très codifiée. La recherche ne faiblit pas pour mettre au point des moyens diagnostiques innovants et des thérapies plus efficaces.
Recherches
Ostéoporose : Mieux comprendre les

Voir la signature
dinouille

dinouille
Membre AmbassadeurBon conseiller
![]()
dinouille
Membre Ambassadeur
Dernière activité le 27/04/2026 à 09:14
Inscrit en 2015
133 819 commentaires postés | 107578 dans le groupe Bon à savoir (pour tous)
31 091 de ses réponses ont été utiles pour les membres
Récompenses
-
Bon conseiller
-
Contributeur
-
Messager
-
Engagé
-
Explorateur
-
Evaluateur
Maladies de la rétine: recréer les cellules perdues par médecine régénérative
Les dégénérescences de la rétine sont des pathologies sévères qui peuvent conduire à la cécité.
Les chercheurs souhaitent pouvoir remplacer les cellules détruites au cours de ces maladies afin de rétablir les fonctions rétiniennes normales.
Ils s’intéressent à des molécules qui, une fois activées dans les cellules souches de la rétine, pourraient stimuler le processus régénératif de ce tissu.
Cette recherche est menée par Diana Garcia Garcia dans l’équipe « Cellules souches et neurogenèse dans la rétine » dirigée par Muriel Perron à l’Institut des neurosciences Paris-Saclay.
Zoom sur les dégénérescences rétiniennes
Les maladies dégénératives de la rétine, comme la dégénérescence maculaire liée à l’âge ou la rétinite pigmentaire, conduisent à la cécité en raison de la perte progressive des photorécepteurs, des cellules nerveuses de la rétine qui transmettent l’information visuelle au cerveau.
La dégénérescence maculaire liée à l’âge (DMLA) est une desmaladies dégénératives les plus fréquentes de la rétine. Première cause de malvoyance après 50 ans dans les pays industrialisés, elle touche 1,5 million de personnes en France. La DMLA étant liée au vieillissement, le nombre de cas va continuer à augmenter dans les années à venir, en raison de l’allongement de l’espérance de vie.D’autres maladies de la rétine sont moins répandues, comme la rétinite pigmentaire par exemple.
Devant la fréquence et la gravité des pathologies dégénératives de la rétine, les chercheurs souhaitent développer des moyens de lutter contre ces maladies.
Régénérer les cellules détruites
Les chercheurs s’intéressent à une stratégie prometteuse : utiliser des cellules souches afin de régénérer les cellules perdues. Si dans certains organes, les cellules souches permettent un renouvellement continu des tissus, les cellules souches de la rétine ont la particularité d’être « quiescentes », en dormance, et donc incapable de compenser d’elles-mêmes les cellules perdues. L’idée de Diana Garcia Garcia et de son équipe d’accueil est de « réveiller » ces cellules souches quiescentes en vue de compenser les dégénérescences rétiniennes. Ceci suppose le prérequis de connaître les mécanismes moléculaires qui régulent leur comportement : c’est ce que compte élucider la chercheuse au cours de ce projet.
Deux molécules en ligne de mire
Diana Garcia Garcias’intéresse plus particulièrement à des molécules appelée Hippo/YAP. Ces dernières auraient un rôle dans la régénération de tissus comme le cœur ou encore le foie. De premiers résultats montrent que leur activation stimulerait la régénération d’organes lésés chez les mammifères. Mais leurs fonctions au cours de la réparation neuronale n’ont pas encore été explorées.
Les chercheurs souhaitent se pencher sur lepotentiel de YAP à stimuler les cellules souches de la rétine et évaluer si cette molécule pourrait constituer une cible thérapeutique pour promouvoir un processus régénératif chez des patients atteints de maladies dégénératives de larétine. Si leurs résultats se confirment, cette approche pourrait constituer une approche innovante pour traiter la maladie.
Voir la signature
dinouille

dinouille
Membre AmbassadeurBon conseiller
![]()
dinouille
Membre Ambassadeur
Dernière activité le 27/04/2026 à 09:14
Inscrit en 2015
133 819 commentaires postés | 107578 dans le groupe Bon à savoir (pour tous)
31 091 de ses réponses ont été utiles pour les membres
Récompenses
-
Bon conseiller
-
Contributeur
-
Messager
-
Engagé
-
Explorateur
-
Evaluateur
Sclérose en plaques
La maladie
Les recherches en cours
Les découvertes
La sclérose en plaques est une maladie au cours de laquelle le système immunitaire s’attaque à la myéline, une gaine située autour des fibres nerveuses et nécessaire à la transmission de l’information nerveuse.
Cette pathologie évolutive peut conduire suivant les patients à l’apparition d’handicaps lourds qui peuvent grandement affecter leur vie quotidienne.
Si des progrès ont été réalisés dans la prise en charge de la maladie, elle reste encore à ce jour incurable, mais la recherche avance pour en venir un jour à bout.
La sclérose en plaques en chiffres
La sclérose en plaques atteint préférentiellement les adultes jeunes, entre 20 et 40 ans. Les femmes sont majoritairement touchées, représentant environ 75 % des cas. La pathologie concernerait 2,3 millions de personnes dans le monde. En France, on estime que 100 000 personnes sont atteintes de sclérose en plaques, 4 000 à 6 000 cas environ se déclarant chaque année. La maladie constitue la première cause de handicap sévère d’origine non traumatique chez les trentenaires.
Qu’est-ce que la sclérose en plaques ?
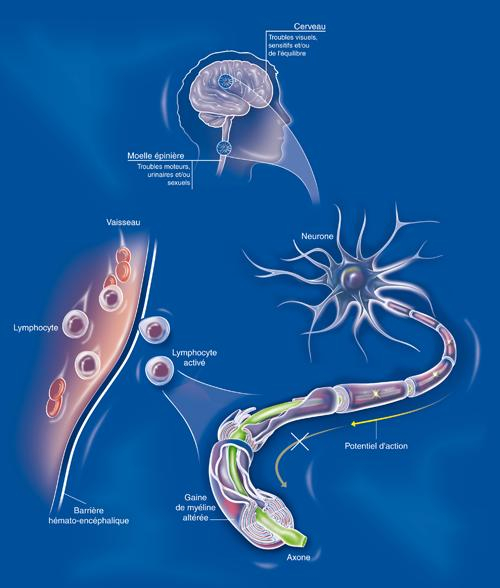
La sclérose en plaques est une maladie auto-immune : le système immunitaire du malade attaque les prolongements des neurones (fibres nerveuses) au niveau du cerveau et de la moelle épinière. Plus précisément, le système immunitaire détruit la myéline, une membrane qui forme une gaine autour des fibres nerveuses et permet une bonne conduction de l’influx nerveux, à l’instar des gaines situées autour des fils électriques. Lorsque la myéline est endommagée, l’information n’est plus transmise correctement. Par ailleurs la destruction de cette myéline entraîne une dégénérescence des fibres nerveuses.
Inserm/Fumat, Carole
Plusieurs types de scléroses en plaques
Classiquement, on distingue deux formes de scléroses en plaques : la forme rémittente et la forme progressive d’emblée. 85 % des scléroses en plaques débutantes sont des formes rémittentes : elles sont caractérisées par une alternance de poussées, c’est-à-dire des phases inflammatoires qui se traduisent par la dégradation de la myéline, et de remyélinisation qui conduit à une régression partielle ou totale des symptômes. Le rythme des poussées varie selon les patients.
Les formes progressives sont plus sévères, et correspondent à une persistance et une aggravation des symptômes. Les formes dites progressives primaires se rencontrent plus fréquemment chez les patients dont la maladie s’est déclarée après 40 ans. Certaines formes rémittentes peuvent peu à peu se transformer en formes progressives, après 10 à 30 ans d’évolution (formes dites secondairement progressives).
Quels sont les facteurs de risque de la sclérose en plaques ?
Les facteurs de risque de la maladie restent méconnus. Des formes familiales de sclérose en plaques ont été identifiées, ce qui a permis de mettre en évidence des facteurs génétiques. Pour l’instant, aucun facteur à lui seul ne permet d’expliquer la survenue de la pathologie : c’est une maladie dite « multifactorielle ». Quelques facteurs de risque ressortent néanmoins comme le tabagisme ou encore une infection par le virus d’Epstein-Bar. De plus, la sclérose en plaques suit une règle dite « gradient Nord-Sud » au niveau mondial : les malades sont plus nombreux dans les pays scandinaves que sur le pourtour du bassin méditerranéen. On évoque ainsi un rôle de l’ensoleillement dans la pathologie.
Quels sont ses symptômes ?
Les symptômes engendrés par la maladie sont très variables et dépendent de la zone où sont situés les neurones dont les prolongements sont touchés par la démyélinisation : problèmes de vue (vision double, perte d’acuité visuelle…), troubles de l’équilibre, déficits moteurs (faiblesse musculaire), sensations perturbées (fourmillements, engourdissements), troubles urinaires ou sexuels. Peuvent s’y ajouter une fatigue générale, des troubles de la mémoire ou de la concentration ou des épisodes dépressifs.
Comment diagnostiquer la maladie ?
Le diagnostic de la maladie peut parfois être long. Il repose d’abord sur un examen neurologique et sur l’imagerie par résonnance magnétique (IRM) qui permet de mettre en évidence les lésions cérébrales générées par la maladie, les fameuses « plaques ». En revanche, ces lésions ne sont pas toujours spécifiques de la sclérose en plaques et leur étendue n’est pas corrélée à la sévérité des symptômes. Une ponction lombaire peut parfois être pratiquée pour rechercher une inflammation au niveau du système nerveux central.
Prise en charge actuelle
Ces dernières décennies, la prise en charge de la sclérose en plaques a été améliorée, l’arsenal thérapeutique s’est étoffé.
Lors des phases de poussées, des corticoïdes sont administrés permettant de réduire leur durée.
Des traitements dits « de fond » ont vu le jour. Ils visent à diminuer la fréquence des poussées et à ralentir la progression de la maladie. Deux grands types de traitement se dégagent :
Les immunomodulateurs (biothérapies) qui visent à freiner le système immunitaire pour limiter l’intensité de la réaction inflammatoire.
Les immunosuppresseurs qui ciblent les cellules immunitaires afin de supprimer totalement la réaction inflammatoire. Leur usage est réservé aux formes les plus graves de la maladie, car elles exposent à un risque d’infections opportunistes, c’est-à-dire des infections ayant lieu lorsque le système immunitaire est moins efficace.
En marge de ces traitements visant à freiner la pathologie, d’autres thérapies ont pour but d’atténuer ses symptômes. La douleur peut être traitée par des antalgiques, et les épisodes dépressifs par des antidépresseurs et une psychothérapie adaptée. En parallèle, une rééducation peut être proposée permettant d’améliorer le quotidien des malades et de leurs proches.
Quels sont les axes de recherche sur la sclérose en plaques ?
La sclérose en plaques fait partie des pathologies mises en avant dans le « plan maladies neurodégénératives 2014-2019 » lancé par le Gouvernement Français. Ce plan va donner un véritable élan aux recherches sur ces maladies et devrait permettre d’améliorer leur prise en charge.
Aujourd’hui, les axes de recherche sur la sclérose en plaques sont multiples. Tout d’abord, les chercheurs veulent identifier des facteurs, environnementaux et génétiques, qui augmenteraient le risque de développer la maladie.
Ils s’attachent également à mieux comprendre les mécanismes de formation de la myéline, en vue de développer des moyens pour la stimuler et réparer ainsi les fibres nerveuses abîmées. Ils s’intéressent aussi aux mécanismes qui régissent sa destruction par le système immunitaire afin de réussir à les contrer.
Enfin, la recherche vise également à améliorer les traitements. Autant de pistes prometteuses pour l’avenir.
Voir la signature
dinouille

dinouille
Membre AmbassadeurBon conseiller
![]()
dinouille
Membre Ambassadeur
Dernière activité le 27/04/2026 à 09:14
Inscrit en 2015
133 819 commentaires postés | 107578 dans le groupe Bon à savoir (pour tous)
31 091 de ses réponses ont été utiles pour les membres
Récompenses
-
Bon conseiller
-
Contributeur
-
Messager
-
Engagé
-
Explorateur
-
Evaluateur
Sclérose en plaques : Etudier les mécanismes de la neurodégénérescence par des techniques avancées d’imagerie
La sclérose en plaques est une pathologie auto-immune qui induit une destruction neuronale à long terme : il n’existe pour le moment pas de traitement contre ce phénomène.
Les mécanismes moléculaires impliqués dans cette dégénérescence neuronale restent méconnus, ce qui nuit à la mise au point de thérapies adaptées.
Une équipe souhaite, à l’aide de technologies d’imagerie de pointe, observer les phénomènes à l’origine de la destruction neuronale pour mieux les combattre.
Cette recherche est menée par Catherine Lubetzki, Bruno Stankoff et leur équipe « Mécanismes de myélinisation et de démyélinisation dans le SNC » à l’Institut du Cerveau et de la Moelle épinière à Paris.
Sclérose en plaques et mort neuronale
La sclérose en plaques est une maladie auto-immune qui touche le système nerveux central (le cerveau et la moelle épinière). Cette pathologie très fréquente toucherait 100 000 personnes dans l’hexagone. Autre caractéristique de la sclérose en plaques : elle se déclare majoritairement chez des personnes jeunes, de 25 à 35 ans.
Lors de cette pathologie, le système immunitaire s’attaque à la myéline, la substance qui entoure le prolongement des neurones et est essentielle à la transmission des messages nerveux.
Cette absence de messages nerveux se traduit par des symptômes variables selon les neurones concernés, allant de déficits moteurs à des troubles sensoriels. La destruction de la gaine de myéline s’accompagne par la suite d’une dégénérescence lente des neurones, source du handicap à long terme.
Aujourd’hui, il existe des traitements qui permettent de diminuer l’inflammation dans la maladie, mais malheureusement, aucun ne parvient à stopper cette dégénérescence.
L’équipe de Bruno Stankoff souhaite mieux comprendre les phénomènes impliqués dans cette destruction afin de mieux les contrer.
Quels sont les mécanismes en cause ?
Les chercheurs suspectent plusieurs mécanismes d’être à l’origine de la dégénérescence neuronale. Le premier résulterait d’une insuffisance de la « remyélinisation spontanée », c’est-à-dire un manque de reformation de la myéline entre deux phases inflammatoires de la pathologie.
Le deuxième serait liée à une inflammation résiduelle au sein du cerveau liée à la suractivation de certaines cellules immunitaires cérébrales appartenant au système immunitaire inné.
Le troisième serait associé à un déficit énergétique des neurones. Autant de pistes à explorer par les chercheurs durant ce projet.
Observer la neurodégénérescence grâce à l’imagerie cérébrale
Malheureusement, l’équipe est confrontée à un véritable problème : les phénomènes impliqués dans la dégénérescence neuronale liée à la sclérose en plaques ne sont pas observables par des méthodes d’imagerie classique comme l’imagerie par résonnance magnétique (IRM).
Les chercheurs vont ainsi s’appuyer sur des techniques d’imagerie de pointe telle que l’ « imagerie par tomographie à émission de positons » ou la « spectroscopie de diffusion » afin d’étudier ces mécanismes sous jacents de la progression à différents stades de la maladie, et ce à un niveau moléculaire.
Il s’agira d’observer la progression de l’atteinte tissulaire cérébrale au cours de la sclérose en plaques en corrélation avec les différents mécanismes précédemment cités à l’aide de marqueurs spécifiques. Cela permettra d’établir la relation entre mécanisme biologique et apparition du handicap neurologique.
Les chercheurs pensent que ces travaux pourraient permettre de grandement faciliter le développement et l’évaluation de futures stratégies thérapeutiques pour combattre la pathologie, et ainsi lutter contre la dégénérescence neuronale qui y est associée.
Voir la signature
dinouille

dinouille
Membre AmbassadeurBon conseiller
![]()
dinouille
Membre Ambassadeur
Dernière activité le 27/04/2026 à 09:14
Inscrit en 2015
133 819 commentaires postés | 107578 dans le groupe Bon à savoir (pour tous)
31 091 de ses réponses ont été utiles pour les membres
Récompenses
-
Bon conseiller
-
Contributeur
-
Messager
-
Engagé
-
Explorateur
-
Evaluateur
Sclérose en plaques : Mieux comprendre les mécanismes de réparation de la myéline pour développer de nouvelles stratégies thérapeutiques
La sclérose en plaques est une pathologie cérébrale caractérisée par une destruction de la myéline, une membrane située autour des fibres nerveuses et nécessaire à la transmission de l’influx nerveux.
Les études ont montré qu’entre deux « poussées » de la maladie, certains patients ont une capacité accrue de réparation de la gaine de myéline.
Les chercheurs souhaitent comprendre comment stimuler cette réparation, pour améliorer les traitements existants.
Cette recherche est menée par Pascale Durbec et son équipe « Cellules souches et réparation du système nerveux adulte » à l’Institut de Biologie du développement de Marseille.
L’importance de la myéline
La myéline est une membrane essentiellement constituée de lipides, qui forme une gaine autour des fibres nerveuses. Elle permet une bonne conduction de l’influx nerveux, à l’instar des gaines situées autour des fils électriques. Lorsqu’elle est endommagée, comme c’est le cas dans la sclérose en plaques, l’information n’est plus transmise correctement, ce qui entraîne la dégénérescence des fibres nerveuses. Des troubles neurologiques apparaissent alors et aboutissent à un handicap important.
Les origines de la sclérose en plaques
La sclérose en plaques est une maladie dite auto-immune : le système immunitaire du malade attaque les fibres nerveuses au niveau du cerveau et de la moelle épinière, plus précisément il détruit la gaine de myéline de ces fibres. Les principaux traitements de la sclérose en plaques visent à moduler le système immunitaire, mais ne permettent pas la guérison. C’est pourquoi il est urgent de développer de nouvelles approches thérapeutiques qui permettront de réparer la myéline autour des fibres nerveuses.
Favoriser la régénération de la gaine
De récents travaux ont montré que la gaine de myéline se régénérait plus efficacement chez certains patients souffrant de sclérose en plaques. La même observation a été faite chez des souris souffrant de la maladie, d’où l’idée de Pascale Durbec et de son équipe de mieux comprendre les mécanismes en jeu chez ces animaux, afin de développer de nouvelles stratégies thérapeutiques.
Chez les souris souffrant de sclérose en plaques, les chercheurs ont identifié deux populations de cellules présentes dans le cerveau, qui participent à la régénération de la myéline. Leur objectif est maintenant de caractériser les mécanismes qui contrôlent cette auto-réparation pour promouvoir la remyélinisation. D’une part, ils analyseront la contribution relative des deux types cellulaires aux processus de réparation, d’autre part ils décrypteront le programme moléculaire qui contrôle la transformation de ces cellules en oligodendrocytes, les cellules qui assurent la formation de la myéline.
Stimuler cette auto-réparation constituerait une approche thérapeutique intéressante de la maladie.
Voir la signature
dinouille

dinouille
Membre AmbassadeurBon conseiller
![]()
dinouille
Membre Ambassadeur
Dernière activité le 27/04/2026 à 09:14
Inscrit en 2015
133 819 commentaires postés | 107578 dans le groupe Bon à savoir (pour tous)
31 091 de ses réponses ont été utiles pour les membres
Récompenses
-
Bon conseiller
-
Contributeur
-
Messager
-
Engagé
-
Explorateur
-
Evaluateur
Pancréas artificiel autonome : une prise en charge prometteuse du diabète
Le diabète de type 1 est une pathologie auto-immune liée à la destruction de certaines cellules du pancréas en charge de la sécrétion d’insuline, l’hormone régulatrice du taux de sucre dans le sang.
Aujourd’hui, les chercheurs souhaitent développer un pancréas artificiel visant à supplanter les fonctions des cellules pancréatiques perdues.
Notre marraine, Marina Carrère d’Encausse, est allée à la rencontre du Pr Eric Renard, véritable pionnier dans le domaine afin de faire le point sur le sujet.
Le Pr Éric Renard dirige depuis 2010 le département d’endocrinologie, de diabétologie et de nutrition de l’hôpital Lapeyronie au CHU de Montpellier. C’est un spécialiste mondialement reconnu dans le développement de nouvelles thérapeutiques pour les diabétiques : il a ainsi coordonné plusieurs essais cliniques de pancréas artificiel.
Marina Carrère d’Encausse : Depuis quelques années, capteurs de glycémie et pompes à insuline ont beaucoup amélioré la vie des patients diabétiques. De quoi s’agit-il ?
Pr Éric Renard : Parce que son pancréas est défaillant, un diabétique de type I est obligé de vérifier sa glycémie (NDLR : son taux de sucre sanguin), en se piquant le bout du doigt, et de s’injecter si besoin une dose d’insuline sous la peau ; et ce, plusieurs fois par jour. Depuis une quinzaine d’années, il existe deux dispositifs qui assurent ces fonctions en continu : un capteur implanté sous la peau qui mesure en temps réel la glycémie et une pompe à insuline qui délivre des doses ajustables grâce à un fin tuyau lui aussi introduit sous la peau. Des milliers de malades dans le monde sont ainsi équipés : en fonction des informations fournies par le capteur, ils ajustent eux-mêmes les doses d’insuline délivrées par leur pompe.
M. C. D’E. : En quoi le pancréas artificiel améliore-t-il ce système ?
E. R. : Le pancréas artificiel permet d’automatiser tout cela en ajoutant au dispositif existant un 3e élément qui joue le rôle de relais d’information entre le capteur qui mesure la glycémie et la pompe qui délivre l’insuline. Ce 3eélément, c’est un programme informatique sophistiqué qui prend la forme d’une application sur smartphone ou tablette. C’est donc le smartphone qui, grâce à ce programme dédié, calcule les doses d’insuline à délivrer à partir des informations fournies par le capteur de glycémie et commande directement la pompe, sans intervention du patient. Les équipes universitaires comme la nôtre, développent des programmes les plus intelligents possible, capables de s’adapter à des situations diverses (sommeil, activité physique, repas…) tout en garantissant une sécurité maximale, car hyper ou hypoglycémies peuvent avoir des conséquences très graves pour les patients.
M. C. D’E. : Votre équipe a été la première à tester un pancréas artificiel en situation de vie réelle. Quels ont été les résultats ?
E. R. : En 2015, nos patients ont testé la machine chez eux pendant deux mois. Le pancréas artificiel était mis en marche uniquement le soir, avant le dîner, et durant toute la nuit. Les résultats ont été très encourageants : cette utilisation a permis de réduire significativement la survenue d’hypoglycémies la nuit. C’est un bénéfice immédiat pour les patients. Par ailleurs, nous avons aussi constaté une amélioration du temps passé avec une glycémie normale et ainsi du contrôle global de leur diabète : leur hémoglobine glyquée était plus basse (NDLR : le taux sanguin d’hémoglobine glyquéereflète l’équilibre glycémique sur une longue période, de 2 à 3 mois).
M. C. D’E. : Les patients ont ensuite testé la machine 24 heures sur 24, comment cela s’est-il passé ?
E. R. : Nous avons coordonné une étude internationale (France, Hollande et Italie) dans laquelle une vingtaine d’adultes a en effet testé dans la continuité de l’étude précédente la machine en continu 24 heures sur 24 durant un mois. Cette étude cumulée, une des plus longues jamais réalisées en conditions de vie réelle, a été publiée l’été dernier. Nos résultats montrent que si la plupart des bénéfices sont obtenus grâce au contrôle nocturne de la glycémie, l’utilisation de la machine dans la journée aussi permet d’améliorer encore le contrôle du diabète en réduisant les écarts glycémiques par rapport à la normale. L’objectif est désormais de tester la machine durant six mois.
M. C. D’E. : Cependant, ce pancréas artificiel a encore des limites… Lesquelles ?
E. R. : Pour l’instant, l’automatisation est incomplète. Le patient doit intervenir avant chaque repas, en indiquant la quantité de glucides qu’il prévoit d’ingérer afin que le programme calcule la bonne dose d’insuline. Cette intervention est nécessaire car l’insuline est injectée dans le liquide interstitiel où baignent les cellules, et non dans le sang directement, comme c’est le cas naturellement avec le pancréas. Du coup, cela met quelques dizaines de minutes avant d’agir réellement sur la glycémie, et donc d’être perçu par le capteur. La mise au point d’une insuline qui agit plus rapidement devrait permettre au pancréas artificiel d’être plus efficace et encore plus autonome. Des équipes de recherche de l’industrie pharmaceutique travaillent sur ce sujet. Pour le reste, beaucoup de progrès ont été faits quant aux machines elles-mêmes. Ainsi, le fabricant américain Medtronic®, l’un des leaders mondiaux en matière de pompe à insuline, prévoit de commercialiser dès cette année une pompe qui renfermera elle-même le programme informatique. Il n’y aura donc plus besoin de smartphone ou de tablette pour faire le lien entre pompe et capteur.
Voir la signature
dinouille

dinouille
Membre AmbassadeurBon conseiller
![]()
dinouille
Membre Ambassadeur
Dernière activité le 27/04/2026 à 09:14
Inscrit en 2015
133 819 commentaires postés | 107578 dans le groupe Bon à savoir (pour tous)
31 091 de ses réponses ont été utiles pour les membres
Récompenses
-
Bon conseiller
-
Contributeur
-
Messager
-
Engagé
-
Explorateur
-
Evaluateur
La stimulation cérébrale : avenir de la neurochirurgie
VOIR AUSSI
Les 10 innovations qui vont révolutionner la médecine
La maladie de Parkinson
Les TOC : l'enfer de l'obsession
Des pacemakers à tout faire !
La chirurgie face à la maladie de Parkinson
Maladies mentales : les traitements de demain
Loin des lobotomies ou autres procédures mutilantes, la stimulation cérébrale offre aujourd'hui de nouveaux horizons à la neurochirurgie. Il est maintenant possible de soulager efficacement des patients atteints de la maladie de Parkinson ou de troubles obsessionnels compulsifs. Cette technique pourrait demain concerner d'autres maladies.
Les yeux ouverts, parfaitement réveillé, Alain est constamment sollicité alors que le chirurgien implante au coeur de son cerveau des électrodes au millimètre près. Cette technique impressionnante a permis à des centaines d'autres patients atteints de la maladie de Parkinson de retrouver une vie normale.
Neurochirurgie : la fin de la mauvaise réputation ?
Fini la lobotomie et autres opérations chirurgicales mutilantes, la stimulation cérébrale permet de redorer le blason d'une discipline qui n'a pas bonne presse. Contrairement aux opérations pratiquées principalement dans les années 1950, la nouvelle technique est pratiquement dépourvue de complications et n'entraîne pas de destructions cérébrales définitives.
Elle consiste à l'introduction de mini-électrodes délivrant des impulsions à haute fréquence au sein d'une zone cérébrale profonde de la taille d'un petit pois. Les stimulations à haute fréquence inhibent les neurones et interrompent la transmission du message nerveux. Le groupement de neurones ciblé intervient dans un contrôle particulier que l'on veut modifier.
ACTUALITÉ DES MARQUES
VOIR LA VIDEO
La fatigue visuelle est due à de nombreux facteurs : nous vous aidons à les identifier rapidement !
La stimulation électrique de ces structures cérébrales modifie leur fonctionnement et améliore les symptômes. Grâce au développement de l'imagerie cérébrale, certaines zones ont pu être identifiée avec précision.
Bien entendu, une fois en place, les stimulations se font sans que le patient n'en soit conscient et les électrodes ne sont pas visibles de l'extérieur. Ce procédé fonctionne sur le même modèle que le pacemaker pour le coeur, les deux électrodes sont reliées au stimulateur placé sous la peau. Pour le moment, cette technique a démontré une certaine efficacité dans le cadre du traitement de la maladie de Parkinson et, par hasard, des troubles obsessionnels compulsifs.
La nécessité d'un suivi rigoureux permet un contrôler régulièrement l'évolution du traitement. En cas de problème, il est possible d'arrêter le traitement en arrêtant les stimulations voire en enlevant les électrodes.
Stimulation cérébrale profonde contre la maladie de Parkinson
Plusieurs centaines de patients souffrant de la maladie de Parkinson avancée ont été traitées avec succès grâce à l'implantation d'électrodes au niveau d'une région du cerveau située sous le thalamus : le noyau sous-thalamique. Ces électrodes sont alors reliées par un câble sous-cutané à un petit boîtier de stimulation placé juste sous la clavicule.
La stimulation a réellement amélioré la qualité de vie des patients en agissant sur la triade des symptômes de la maladie de Parkinson : les tremblements, la raideur et la difficulté à contrôler ses mouvements. La stimulation profonde n'est indiquée qu'à des malades depuis plus de 5 ans. Aujourd'hui, en France, seule une quinzaine de centres réalisent ce type d'intervention de neurochirurgie. Et malheureusement, un nombre restreint de malades a accès à cette technique, en raison de la lourdeur de l'intervention et de son coût très élevé.
Plus récemment, une équipe du Groupe hospitalier de la Pitié-Salpétrière ont fortuitement découvert une nouvelle application à cette technique. Au cours de l'enquête psychologique précédant l'intervention, les chercheurs ont constaté la présence de troubles obsessionnels compulsifs chez deux parkinsoniens. Les deux patients opérés et suivis par l'équipe de la Salpetrière, ont vu leurs TOC quasi disparaître. 18 mois après l'intervention, l'arrêt de ces troubles psychiatriques est toujours observé.
Quant à leur maladie de Parkinson, l'amélioration des troubles moteurs a été presque complète chez l'un des malades, et seulement partielle chez l'autre. Bien que ne concernant que deux personnes, cette observation suggère que l'électrostimulation peut agir non seulement sur des symptômes neurologiques mais également des phénomènes psychiatriques.
Vers des applications contre les maladies psychiatriques ?
Spécialiste du traitement neurochirurgical de la maladie de Parkinson, le Pr. Alim-Louis Benabid avait saisi en octobre 2001 le Comité Consultatif national d'éthique (CCNE) sur les implications éthiques liées au développement de nouvelles applications de ce traitement. En juin 2002, le CCNE donnait son feu vert de principe tout en fixant des limites assez strictes. Vis-à-vis d'autres applications possibles (dépressions graves résistantes au traitement, psychoses schizophréniques résistantes au traitement…), le comité émet des réserves, en l'absence d'études complémentaires. Dans tous les cas, un encadrement très strict de ces pratiques, la mise en place d'un comité de contrôle et l'acceptation du traitement par le malade sont essentiels. Ces restrictions devraient, selon le CCNE, éviter les risques de dérives.
L'intérêt scientifique pour cette technique est très élevé. Lors du troisième forum européen sur les neurosciences en juillet 2002, le Pr. Benabid rappelait que les chercheurs ont évoqué une large gamme d'applications potentielles dans des cas aussi variés que l'épilepsie et l'obésité due à un dysfonctionnement endocrinien. Le professeur avait également évoqué de possibles applications préventives : "Des expériences sont par ailleurs en cours de réalisation pour envisager les façons d'utiliser cette technique pour développer des méthodes neuroprotectrices. Ces dernières pourraient servir à empêcher les lésions du système nerveux, et donc les troubles neurologiques".
Ecrit par:
David Bême
Voir la signature
dinouille
Donnez votre avis
Articles à découvrir...

18/04/2026 | Nutrition
Entre promesses et réalité : les oméga-7 peuvent-ils améliorer la santé métabolique ?
S'abonner
Vous souhaitez être alerté des nouveaux commentaires
Votre abonnement a bien été pris en compte







dinouille
Membre AmbassadeurBon conseiller
dinouille
Membre Ambassadeur
Dernière activité le 27/04/2026 à 09:14
Inscrit en 2015
133 819 commentaires postés | 107578 dans le groupe Bon à savoir (pour tous)
31 091 de ses réponses ont été utiles pour les membres
Récompenses
Bon conseiller
Contributeur
Messager
Engagé
Explorateur
Evaluateur
Un nouveau test sanguin utilise l’ADN pour détecter de nombreuses maladies
FacebookPin ItE-mailPlus
L’analyse ADN d’une seule goutte de sang permettrait de détecter de nombreuses maladies, à l’image du cancer du pancréas, la sclérose en plaques ou le diabète. Ce nouveau test sanguin utiliserait l’ADN de cellules mourantes pour détecter les pathologies.
Jusqu’ici, le test sanguin permettait :
– de repérer les premiers stades d’une pathologie comme le développement d’une tumeur cancéreuse ou d’une maladie auto-immune ou neurodégénérative comme Alzheimer.
– de déterminer la progression d’une pathologie
– le succès d’une thérapie ou ses effets toxiques.
Le principal problème était de ne pouvoir déterminer l’organe auquel appartenaient les cellules, ce qui nécessitait donc un examen invasif.
Pour cette raison, des chercheurs de l’Hebrew University de Jérusalem ont effectué une série d’expériences sur 320 patients.
Ainsi le nouveau test sanguin élaboré permet désormais de détecter les tissus spécifiques dans lesquels les cellules mourraient, à partir de deux principes biologiques :
– les cellules mourantes libèrent des fragments d’ADN circulant un court moment dans le sang. Un procédé connu depuis des décennies, mais il était jusqu’ici impossible de déterminer le tissu d’origine.
– L’ADN porte une marque chimique unique appelée méthylation, stable dans les tissus sains comme dans les malades.
Ruth Shemer, coauteur de l’étude explique : « nos travaux démontrent qu’il est possible d’identifier de quels tissus dans l’organisme proviennent les fragments d’ADN qui circulent dans le sang ».
« Cela représente une nouvelle méthode pour détecter des cellules mourantes dans des tissus spécifiques et une approche très prometteuse pour diagnostiquer des maladies ».
Benjamin Glaser, professeur et patron du département d’endocrinologie au centre médical Hadassah à Jérusalem ajoute même : « à plus long terme, nous envisageons un nouveau test sanguin capable de détecter des dommages dans des tissus même sans suspecter a priori que des maladies touchent un organe spécifique ».