Quels sont les différents types d'essais cliniques ?
Publié le 24 avr. 2021 • Par Équipe éditoriale de Carenity
En fonction de la pathologie et du médicament, les essais cliniques auront pour but de mettre en évidence des paramètres différents.
Mais alors quels sont les différents essais cliniques aujourd’hui pouvant être réalisés avant et après la commercialisation d’un médicament?
On vous dit tout dans notre article !

Le développement d’un médicament est un processus long et complexe. Il est soumis à différentes études avant de pouvoir être commercialisé sur le marché. Ces études se divisent en 3 phases : la phase de recherche, la phase de développement, durant laquelle s’effectue les études précliniques et cliniques, puis la phase de commercialisation avec sa mise sur le marché et son suivi en temps réel. Après sa commercialisation différentes études peuvent être réalisées comme c’est le cas sur Carenity !
Les recherches impliquant la personne humaine
La réalisation d’un essai clinique repose sur le respect de la personne humaine. On peut distinguer trois catégories de recherches impliquant la personne humaine :
- Les recherches interventionnelles, dites de catégorie 1 : elles portent sur un médicament, ou sur des dispositifs médicaux. (Exemple : étude d’une nouvelle molécule)
- Les recherches interventionnelles avec des risques et contraintes minimes, dites de catégorie 2 : elles portent sur l’utilisation de produits de santé dans les conditions habituelles d’utilisation. (Exemple : comparaison entre deux traitements pour l’hypertension artérielle).
- Les recherches non interventionnelles, ou observationnelles, dites de catégorie 3 : elles ne comportent aucun risque pour la personne, et consiste à suivre le patient utilisant le produit normalement. Ce sont des études qui consistent à observer l’association de facteurs à des évènements de santé. En aucun cas il s’agit d’une étude expérimentale. (Exemple : incidence de cancer du poumon chez les fumeurs et non fumeurs).
Les différents essais des recherches interventionnelles
Avant le début de l’essai, les patients seront répartis en différents groupes de manière aléatoire ou non. C’est à dire, par tirage au sort, ou à l’inverse en connaissance de leur traitement
Durant l’essai les patients seront comparés:
- A un traitement de référence, dans le cas où l’objectif de l’étude serait d’évaluer un médicament par rapport à un autre
- À un placebo, qui est une substance sans principe actif qui peut avoir un effet psychologique sur le patient, dans le cas où l’objectif serait d’évaluer les propriétés du médicament en lui-même
- Sans comparaison directe
Le design de l’essai va être fait en fonction des objectifs et des caractéristiques à mettre en avant.
Comment l’essai peut alors se dérouler?
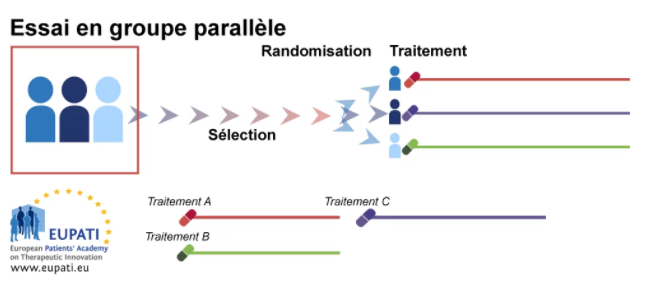
Essai en parallèle: les patients seront attribués aléatoirement dans des groupes différents. Ils seront suivis tout au long de l’essai dans ce même groupe.
Cet essai peut être réalisé afin de comparer un médicament/un placebo ou deux médicaments. On peut également comparer un même médicament dans des groupes présentant des facteurs distincts (exemple : homme et femme).
Les groupes seront alors comparés les uns aux autres.
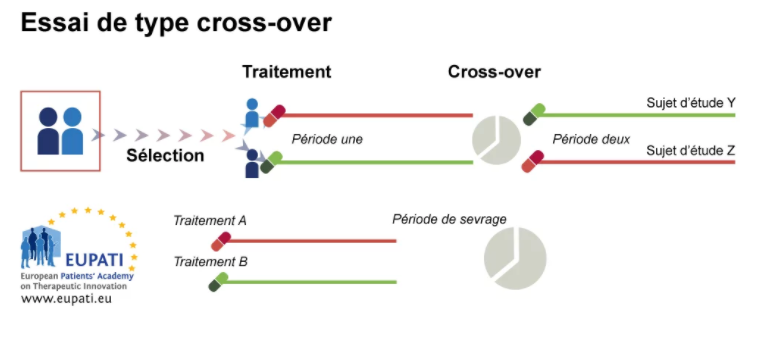
Essai en cross-over: les groupes recevront chaque traitement les uns à la suite des autres. Le groupe A commencera par le traitement A et le groupe B par le traitement B durant la première phase de l’essai, puis lors de la seconde phase, le groupe A recevra le traitement B et le groupe B recevra le traitement A.
L’ordre d’attribution des traitements sera fait de façon aléatoire. Pour cet essai chaque patient sera son propre témoin.
Cependant, cette étude est longue car une période de “washout” sera réalisée entre les deux phases, c'est-à- dire un laps de temps durant lequel le patient ne reçoit aucun traitement.
Essai séquentiel: les patients reçoivent un premier traitement puis un second traitement avec une période de washout entre les deux. La différence est qu’ici il n’y aura pas de comparaison groupe A et groupe B.
Il existe une notion très importante pour parler d’un essai clinique. En fonction du design d’attribution du produit de santé, on dit que l’essai est réalisé:
- En ouvert: c'est-à-dire que l’investigateur et le patient savent tous les deux le traitement reçu. Cela peut néanmoins engendrer des erreurs lors de l’analyse des résultats. En effet, s’il est dit à un patient qu’il prend un placebo, celui-ci se dira directement qu’aucun résultat ne sera possible. Il en est de même pour l'interprétation des résultats si l’investigateur connaît l’attribution des traitements.
- En simple aveugle: un des deux ne connaît pas le traitement reçu.
- En double aveugle: ni le patient, ni l’investigateur ne connaissent l’attribution du traitement. Il s’agit de la méthode recommandée car elle permet de limiter au maximum les faux résultats.
Les différents essais dans les recherches observationnelles:
Tout d'abord, il faut savoir qu’une étude observationnelle est réalisée à un instant donné. Il s’agit d’un recueil d’informations de la part des patients qui peut être fait de manière:
- Rétrospective: l’essai se déroule après le déroulement des événements étudiés.
- Prospective: l’essai se déroule avant le déroulement des événements étudiés.
Le design peut, là aussi, être différent en fonction de ce qu’on souhaite mettre en avant:
- L’étude de cohorte : qui permet de mesurer l’association entre une exposition (exemple : fumeurs/non fumeurs) et un événement (exemple : cancer du poumon). Les patients seront répartis dans des groupes en fonction de leur exposition (les fumeurs sont comparés aux non fumeurs).
- L’étude cas / témoins : qui permet de mesurer l’association en fonction du taux d’exposition (fumeurs/ non fumeurs) chez les cas (malades) et chez les témoins (non malades). Les patients seront répartis en fonction de la réalisation ou non de l'événement (exemple : malades/non malades).
- L’étude transversale : pour une proportion donnée de patients, on va recueillir simultanément les informations concernant la survenue de l'événement et l’exposition afin d’en obtenir une donnée chiffrée (exemple : nombre de personnes atteintes du cancer du poumon et nombre de fumeurs)
- L’étude longitudinale : les informations sont récoltées dans le temps (exemple : suivi de la glycémie chez un patient diabétique).
Les essais cliniques reposent sur le respect du patient et sont primordiaux pour l’amélioration continue des produits de santé. Leur déroulement varie en fonction des objectifs, qu’ils soient expérimentaux ou seulement observationnels.
Cet article vous a-t-il été utile ?
Partagez votre ressenti et vos interrogations avec la communauté en commentaire ci-dessous !
Prenez soin de vous !
Sources :
- Les différents types d’essais cliniques et l’encadrement législatif, Centre Hospitalier_ARRAS
- Méthodologie des essais cliniques, EUPATI
- Définitions des essais cliniques, Remede
2 commentaires
Vous aimerez aussi

Déserts médicaux : quand l’accès aux soins devient un parcours du combattant
7 mars 2025 • 6 commentaires

Le “pacing”, une stratégie essentielle pour mieux vivre avec une maladie chronique
27 déc. 2024 • 18 commentaires

Renforcer son périnée : pourquoi c'est essentiel pour les femmes et les hommes ?
17 déc. 2024 • 6 commentaires

 Facebook
Facebook Twitter
Twitter

